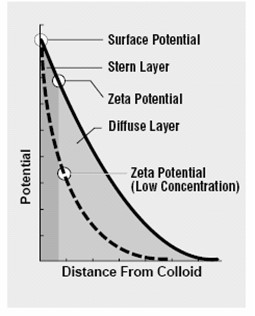
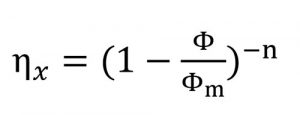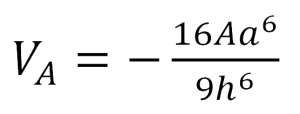عوامل موثر بر خواص رئولوژیکی دوغاب های سرامیکی
الف) گرانروی فاز مایع
گرانروی دوغاب ها به طور مستقیم با گرانروی فاز مایع ارتباط دارد. و برای مثال با فرض ثابت نگه داشتن تمامی پارامترها، با افزایش گرانروی فاز مایع، گرانروی دوغاب افزایش خواهد یافت {F.Liu, 2000}.
ب) غلظت حجمی مواد جامد
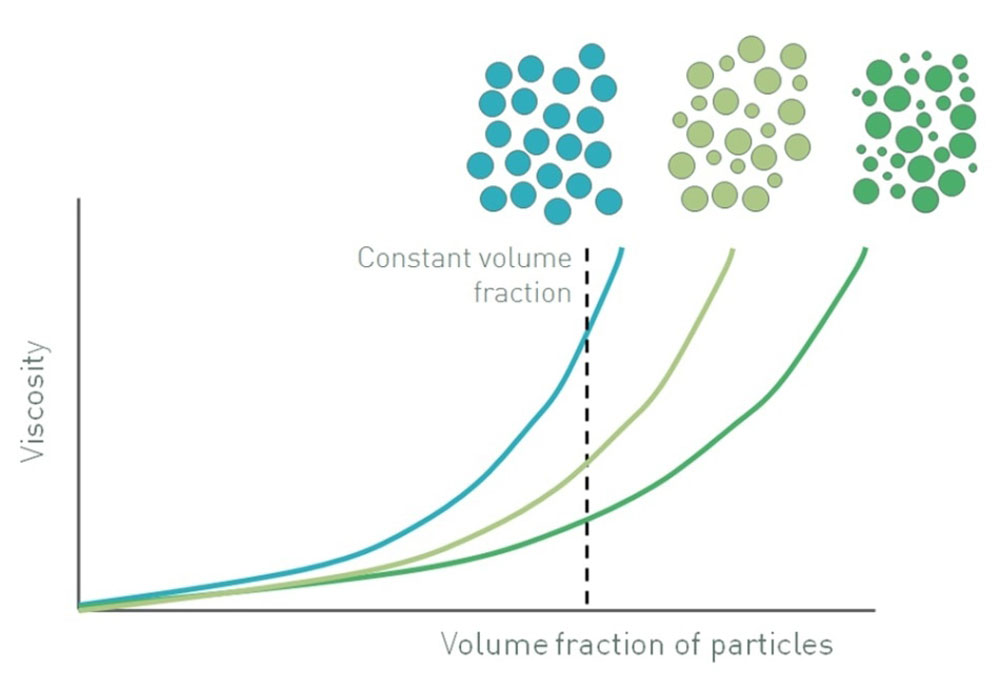
غلظت حجمی مواد جامد عبارتست از حجم کل ذرات به حجم دوغاب که این عامل نقش اساسی در رئولوژی دوغاب ایفا می کند {F.Moore, 1965}. هرچه غلظت ذرات جامد بیشتر باشد، سیال کمتری جهت حرکت دادن ذرات روی هم وجود خواهد داشت که در این حالت گرانروی دوغاب بالاتر خواهد بود تا جایی که گرانروی در یک غلظت حجمی بیشینه (ϕmax) به بی نهایت می رسد.
حداکثر غلظت حجمی وابسته به توزیع اندازه ذرات و شکل و اندازه آن ها می باشد. یک توزیع وسیع اندازه ذرات باعث افزایش مقدار ϕmax می شود. در این حالت ذرات کوچک می توانند در میان حفرات ذرات بزرگ قرار گیرند {F.Liu, 2000}. در مورد شکل ذرات باید گفت که در سوسپانسیون های حاوی ذرات غیرکروی به هنگام چرخش، حجم قابل ملاحظه ای از ذرات به حركت آورده می شود لذا ناحیه آشفته حاصل از یک ذره غیرکروی بیشتر از یک ذره کروی با حجم یکسان است بنابراین می توان گفت ϕmax برای ذرات کروی بیشتر می باشد. رابطه Krieger-Dougherty نشان می دهد که با افزایش کسرحجمی ذرات، گرانروی افزایش می یابد {B.Bengisu, 2001} . در این رابطه ϕm غلظت حجمی بیشینه، ϕ كسر حجمی ذرات است.
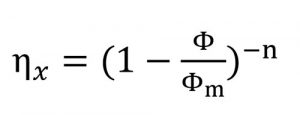
ج) اندازه ذرات
معمولا در دوغاب های سرامیکی ذرات کوچکتر از 10µm و بویژه ذرات کلوئیدی نقش بسزایی دارند {J.S.Reed, 1998}.ذرات دیگر موجود در دوغاب قادر به تغییر رفتار جریانی دوغاب نبوده و تنها با افزایش درصد مواد جامد گرانروی افزایش می یابد. گرانروی دوغاب ها معمولاً با افزایش قطر ذرات تا حدود 10µm به دلیل کاهش نیروهای بین ذرات کاهش می یابد و پس از عبور از حد مذکور، در اثر تضعیف نیروهای بین ذرات و نیز به دلیل متناسب بودن انرژی لازم جهت تحرک ذرات با جرم آن ها، گرانروی افزایش می یابد {F.Moore, 1965}.
د) شکل ذرات
هرچه ذرات به لحاظ شكل نامتقارن تر باشد، انباشتگی آنها بر روی یکدیگر، مشکل تر و در نتیجه غلظت حجمی آنها کمتر و گرانروی بیشتر است. به طور کلی در یک غلظت حجمی ثابت، گرانروی اشكال هندسی مختلف به ترتیب از کره، بیضوی، ذرات نامنظم کروی، ذرات دیسکی شکل و ذرات میله ای شکل افزایش می یابد {F.Moore, 1965}.
ه) نیروهای بین ذرات
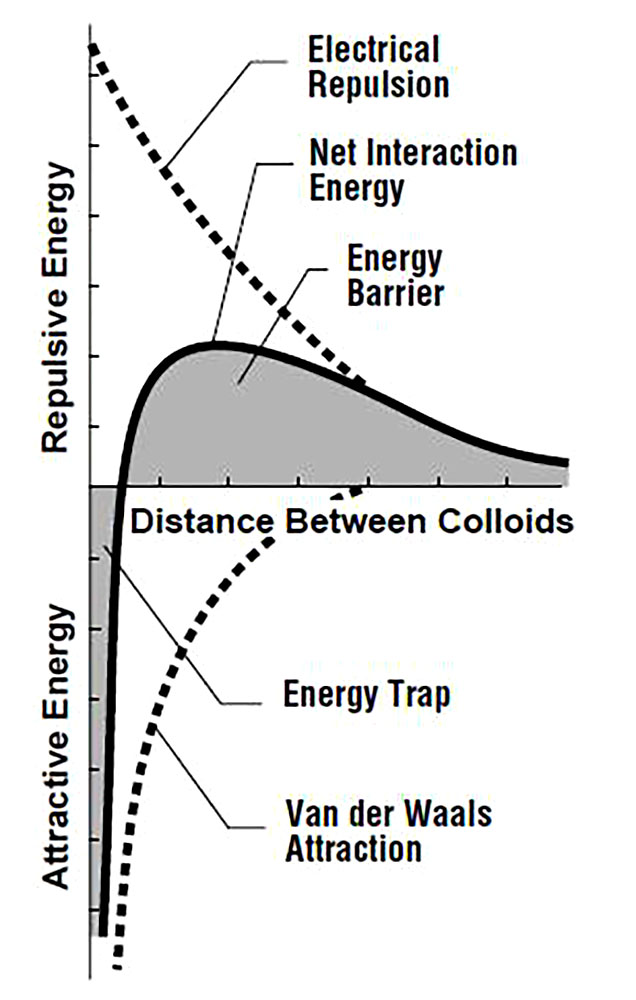
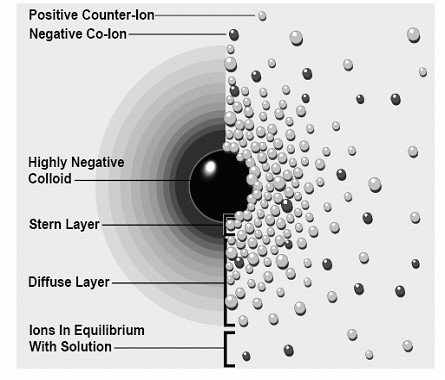
در مورد ذرات واقع در محدوده اندازه کلوئیدی (کمتر از 1µm)، اندازه و بزرگی نیروی بین ذرات تاثیر اساسی بر رفتار سوسپانسیون و رفتار رئولوژیکی آن خواهد داشت. نیروهای موجود در بین ذرات به دو دسته نیروهای جاذبه و نیروهای دافعه تقسیم می شوند. عمده ترین نیروی جاذبه میان ذرات نیروی واندروالس می باشد كه این نیرو به اندازه، شکل ذرات و فاز مایع وابسته است. نیروهای دافعه شامل نیروی دافعه الکترواستاتیک است که این نیرو ناشی از حضور بار در فصل مشترک جامد – مایع است. در واقع بین لایه های مضاعف دو ذره، برهم کنشی ایجاد می شود که به علت همنام بودن بارها این نیرو دافعه خواهد بود. با نزدیک شدن ذرات نیروی دافعه سرانجام در نقطه ای توسط جاذبه واندروالس خنثی می شود. دیگر نیروی دافعه می تواند نیروی دافعه استریک یا ممانعت فضایی باشد که توسط زنجیرهای پلیمری جذب شده، ایجاد می شود. زمانی که در یک دوغاب، میانگین انرژی از نوع دافعه باشد گرانروی سیستم کاهش می یابد {M.N.Rahaman, 2003}.
و) افزودنی ها (چسب ها)
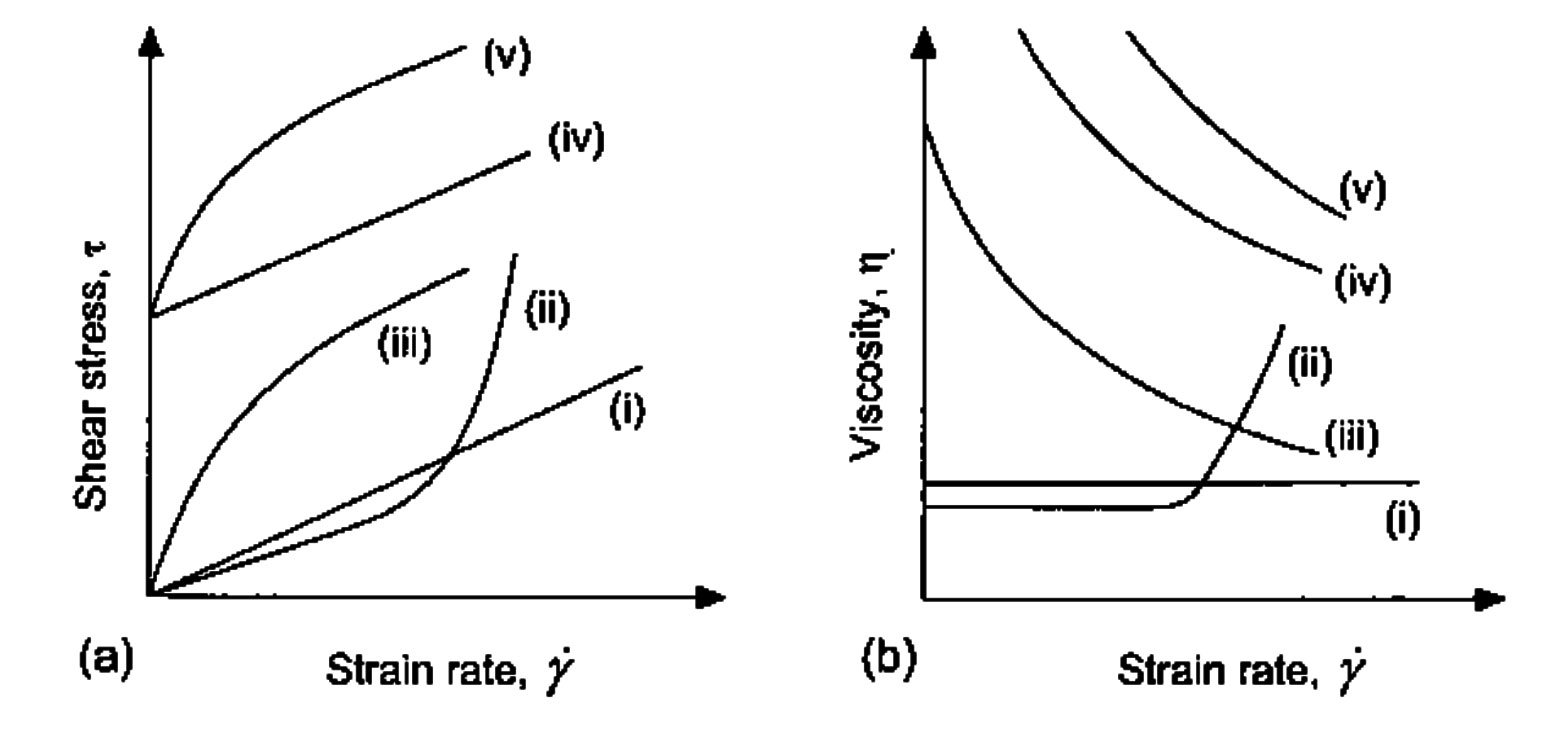
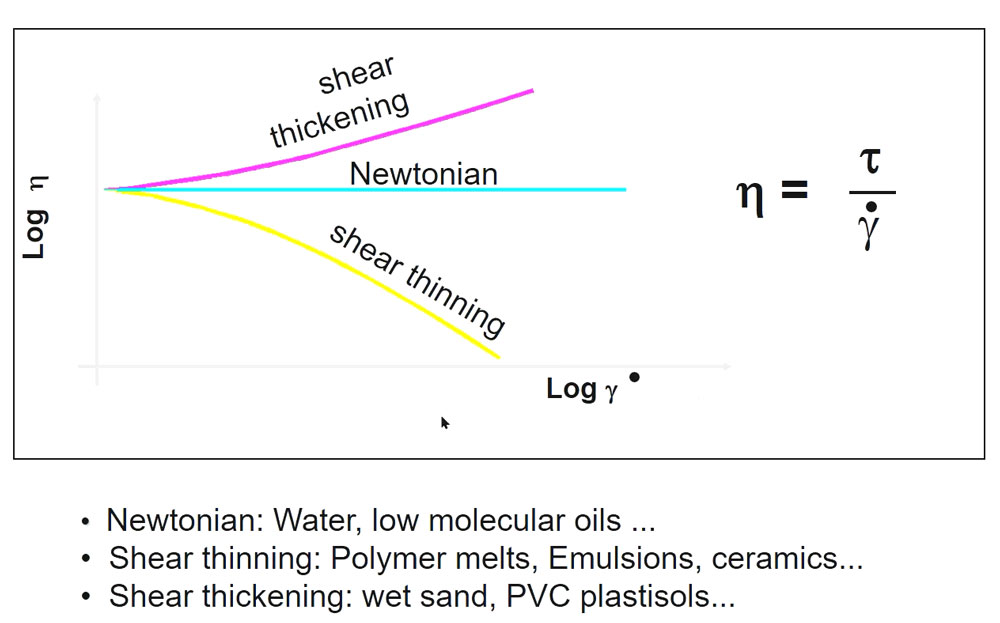
چسب ها نیز بر گرانروی تاثیر دارند و حتی ممکن است ویژگی جریانی دوغاب را از حالت نیوتنی به شبه پلاستیک تبدیل می کنند. اغلب چسبهای آلی، مولکولهای پلیمری با زنجیره بلند هستند. گرانروی دوغاب وابسته به درصد وزنی چسب ) c ( که طبق رابطه زیر به دست می آید{J.S.Reed, 1998;شریفی, 1386}.
Logη=kc